
Fuentes: OMS, Agencia Española del Medicamento, Rtve, Farmaindustria
La investigación en torno al Covid19
Las investigaciones que se están llevando a cabo en el mundo, de manera acelerada, en el ámbito del Covid19 se enfocan sustancialmente en tres áreas: a) Vacunas, b) Tratamientos y c) Estudios observacionales.
En españa, actualmente, existen 10 investigaciones en marcha sobre vacunas, 95 ensayos clínicos solicitados para tratamientos terapéuticos y 132 estudios observacionales.
Vacunas: Son preparaciones biológicas capaces de generar inmunidad contra una enfermedad estimulando la producción de anticuerpos dentro del organismo. Habitualmente, se basan en el microorganismo patógeno (bacterias o virus), muerto o debilitado, sus toxinas o alguna de sus proteínas. Este proceso estimula el sistema inmunológico para que sea capaz de reconocer más adelante al agente patógeno como una amenaza y destruirlo, después de generar lo que se conoce como "memoria inmunológica". Las vacunas se usan con carácter profiláctico, para prevenir o restar agresividad a futuras infecciones.
Tratamientos: Medicamentos, basados en nuevas moléculas o en fármacos ya utilizados para otras enfermedades, que puedes ser eficaces para luchar contra el Covid19. Típicamente trabajan en tres direcciones: a) frenar el propio virus (antivirales), b) paliar la respuesta inmunológica exagerada (antiinflamatorios e inmunosupresores) y c) dirigir el sistema inmunológico (anticuerpos)
Estudios observacionales: Son investigaciones complementarias que se llevan a cabo en muchos hospitales por los propios profesionales clínicos, en las que se recogen datos de salud de los pacientes con el fin de analizar el uso, la seguridad o la efectividad de los
medicamentos en el contexto de la asistencia sanitaria real.
 Las terapias para el tratamiento de la enfermedad constituyen el mayor número de investigaciones que se están llevando actualmente. Se calcula que a nivel internacional hay alrededor de 200 medicamentos en vías de investigación para combatir el Covid19. En España han sido aprobados para ensayos en fase clínica (pruebas con humanos) 95 proyectos, que investigan la eficacia de fármacos conocidos (reposicionamiento), el descubrimiento de nuevas moléculas terapéuticas, o la actividad de nuevas aproximaciones, como por ejemplo el uso de gammaglobulinas o la aplicación de células mesenquimales extraídas de médula ósea o de tejido adiposo. Entre los fármacos conocidos para otras enfermedades de los que se está investigando su potencial aplicación en el ámbito del Covid19, figura por ejemplo el Remdesivir (antiviral), Sarilumab (anticuerpo), Bunesonida (corticosteroide), metilprednisolona (esteroide inmunosupresor), melatonina (hormona natural), Colchicina (antiinflamatorio específico para la gota), Colecalciferol (vitamina D3), Canakinumab (antiinflamatorio para enfermades autoinmunes), ciclosporina (inmunosupresor utilizado en trasplantes),...
Las terapias para el tratamiento de la enfermedad constituyen el mayor número de investigaciones que se están llevando actualmente. Se calcula que a nivel internacional hay alrededor de 200 medicamentos en vías de investigación para combatir el Covid19. En España han sido aprobados para ensayos en fase clínica (pruebas con humanos) 95 proyectos, que investigan la eficacia de fármacos conocidos (reposicionamiento), el descubrimiento de nuevas moléculas terapéuticas, o la actividad de nuevas aproximaciones, como por ejemplo el uso de gammaglobulinas o la aplicación de células mesenquimales extraídas de médula ósea o de tejido adiposo. Entre los fármacos conocidos para otras enfermedades de los que se está investigando su potencial aplicación en el ámbito del Covid19, figura por ejemplo el Remdesivir (antiviral), Sarilumab (anticuerpo), Bunesonida (corticosteroide), metilprednisolona (esteroide inmunosupresor), melatonina (hormona natural), Colchicina (antiinflamatorio específico para la gota), Colecalciferol (vitamina D3), Canakinumab (antiinflamatorio para enfermades autoinmunes), ciclosporina (inmunosupresor utilizado en trasplantes),...
El fármaco conocido que más ensayos clínicos tenía aprobados en España (hasta veinte), la hidroxicloroquina, acaba de ser desestimado por la Agencia Española del Medicamento, ante la evidencia publicada por la OMS de que no es eficaz en el ámbito del Covid19.
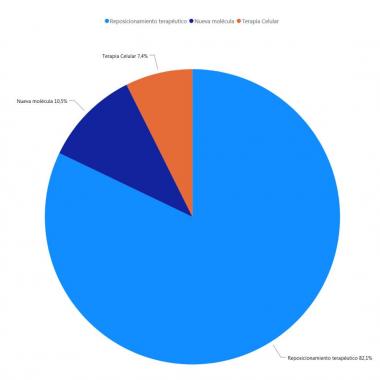
En la figura de la izquierda se ve la distribución de los 95 proyectos de fármacos autorizados para ensayos clínicos actualmente en España. Como se observa, la inmensa mayoría (82%) correponde a reposicionamiento de medicamentos ya existentes, mientras que solamente el 10% están en nuevas moléculas y finalmente, el 8% tiene que ver con terapias celulares.
La ventaja de investigar la posible utilidad de fármacos usados en otras patologías es que ya han sido ensayados y probados, por lo que su toxicidad y su mecanismo de acción es perfectamente conocido y controlado, mientras que la investigación en una nueva entidad terapéutica supone realizar un conjunto de ensayos en laboratorio, animales y humanos que pueden prolongar la investigación durante bastantes años.
En el mundo hay en este momento un total de unos 1.700 ensayos clínicos aprobados para que puedan probarse en humanos, la inmensa mayoría de ellos con fármacos ya conocidos.
De los 95 ensayos clínicos autorizados hasta la fecha en España, el 75% corresponde a promotores públicos (Centros de Investigación, Hospitales) y 25% a organizaciones comerciales (empresas farmaceúticas y biotecnológicas). En cuanto a la situación del ensayo a fecha de hoy, el 6% ha completado el reclutamiento de voluntarios, el 48% está en fase de reclutamiento y el 46% restante aun no ha iniciado la fase de reclutar voluntarios. Finalmente, indicar que participan un total de 159 centros de todo el territorio nacional, correspondiendo la mayoría a Madrid (38), seguido de Cataluña (27) y Andalucía (21).
El largo proceso de la investigación biomédica
Antes de cualquier prueba clínica en humanos, el fármaco candidato debe superar una Fase Preclínica Regulatoria, que incluye pruebas de laboratorio en tejidos aislados y en sistemas vivos completos (gusano, mosca, ratón, rata,...etc.). En esta fase se persiguen diferentes objetivos fundamentales:
a) reconocer el mecanismo de acción;
b) comprender la farmacocinética del producto (capacidad del fármaco de llegar a su objetivo terapéutico antes de que sea metabolizado por el cuerpo);
c) comprender la farmacodinámica del producto (efectos del fármaco sobre el cuerpo humano);
d) Obtener una prueba de concepto positiva;
e) asegurar una toxicidad baja y en todo caso controlada;
f) verificar razonablemente la eficacia del producto en animales;
g) asegurar que se puede fabricar de acuerdo a pautas GMP (Good Manufacturing Practices).
Solo cuando se ha completado la Fase Preclínica y los resultados han sido revisados cuidadosamente por la Agencia del Medicamento, se recibe la autorización para pasar a ensayos clínicos, es decir, con humanos.
Normalmente los ensayos clínicos se realizan en tres fases, seguidos de una fase de seguimiento posterior a la comercialización.
Fase I: El fármaco se prueba en un pequeño conjunto de personas sanas (menos de 100 normalmente) para confirmar la seguridad (es decir, la no toxicidad). En esta fase se busca identificar posibles efectos secundarios y se intenta encontrar la dosis óptima.
Fase II: Es un estudio a mayor escala en el que participan varios cientos de personas. Aquí se evalúan los efectos secundarios más comunes en el corto plazo y cómo reacciona el sistema inmune. Se reclutan voluntarios tanto sanos como enfermos y se confirma la dosis, la no toxicidad y la eficacia.
Fase III: Es un ensayo mucho más grande en el que participan varios miles de voluntarios, generalmente procedentes de diversos países y razas. Se realizan pruebas con grupos sanos, grupos enfermos y grupos de control con placebo. Se recolectan y analizan cuidadosamente datos estadísticos acerca de la efectividad y la seguridad. Esta fase también sirve para detectar otros posibles efectos secundarios que hayan pasado desapercibidos en la Fase 2. Muchos fármacos que superaron las Fase II se caen en la Fase III.
Se comprende que, hasta cierto punto, hay que contar irremediablemente con dos elementos sustanciales: FINANCIACIÓN (completar todas las fases de la investigación en un nuevo medicamento puede costar más de 100 millones de euros) y TIEMPO (se requieren plazos mínimos para verificar el efecto de un nuevo fármaco en el cuerpo humano, cómo reacciona, que efectos secundarios puede producir,...etc.)
Lo dicho hasta aquí para los nuevos candidatos a medicamento vale en gran medida para la investigación en vacunas. Puesto que el mecanismo de acción de una vacuna es por lo general bien conocido y no resulta muy complejo, los tiempos se pueden acortar bastante. En último término la vacuna no es un medicamento, sino un mero estimulante del sistema inmunitario, que es realmente quien realiza la tarea. Los riesgos suelen ser menores y mejor controlados.
Y hablando de vacunas
Actualmente la OMS informa de que existen en el mundo 128 proyectos de vacunas contra el Covid19, que están trabajando a marchas forzadas para completar la fase PRECLÍNICA, y 13 proyectos de vacunas que ya han completado exitosamente esta fase y han entrado en ensayos clínicos. Estos, los más avanzados, son los siguientes:
- CanSino Biological Inc. / Instituto de Biotecnologías de Pekín (China). Fase 2: Se trata de una vacuna de vector viral. Al ser una fórmula de nueva generación que no contiene patógenos, se caracteriza por su seguridad. Las primeras pruebas en personas han resultado satisfactorias y ahora se ha ampliado la muestra para seguir comprobando su eficacia y seguridad.
- Moderna / Instituto Nacional de enfermedades infecciosas NIAID (Estados Unidos), Fase 2: Esta vacuna está basada en ARN mensajero, combinado con el código genético del virus. La farmacéutica estadounidense que la está desarrollando ha informado que en julio comenzaría la tercera y última fase, en la que participarán unas 30.000 personas. La biotecnológica finalizó el mes pasado su fase II del estudio con 300 adultos.
- Sinopharm / Instituto de Productos Biológicos de Wuhan y Sinopharm / Instituto de Productos Biológicos de Pekín (ambos en China). Fase 1/2: China también está desarrollando otros dos proyectos independientes entre sí y muy prometedores. Ambos se basan en virus inactivados y detrás de ellos está Sinopharm, el gigante farmacéutico de carácter estatal. Empezaron a inocularse en humanos el pasado mes de abril y, según fuentes oficiales del país asiático, "han mostrado una adecuada seguridad hasta ahora". La propia Sinopharm ha adelantado que, de continuar así, aproximadamente en mayo de 2021 se podrían completar todos los ensayos clínicos que permitan certificar la seguridad y eficacia de ambos.
- Sinovac (China). Fase 1/2: La cuarta propuesta china parte de virus inactivos purificados, y ha generado muchas expectativas, especialmente después de un estudio publicado en la revista Science sobre los resultados iniciales obtenidos. Al parecer, esta vacuna es capaz de producir anticuerpos efectivos contra el coronavirus en ratones, ratas y macacos. Está previsto que se realicen ensayos clínicos en humanos a lo largo de este año.
- Instituto Jenner de la Universidad de Oxford (Reino Unido). Fase 2b/3: En este proyecto, el más importante que se está llevando a cabo en suelo europeo, también participa la multinacional farmacéutica AstraZeneca. Utiliza una versión modificada de adenovirus y ya han comenzado los ensayos en humanos voluntarios. Los investigadores estiman su probabilidad de éxito en un 80%, y creen que para finales de 2020 podría estar ya lista una vacuna para uso limitado. Incluso han llegado a afirmar que los británicos podrían tener acceso a una posible vacuna contra el coronavirus a partir del próximo septiembre, si progresan los ensayos. Alemania, Francia, Italia y Países Bajos han firmado un precontrato con AstraZeneca para el suministro de hasta 400 millones de dosis de esta vacuna, destinadas a toda la población de la UE.
- BioNTech / Fosun Pharma / Pfizer (Alemania / Estados Unidos). Fase 1/2: La compañía alemana BioNTech se alió en enero con la farmacéutica estadounidense Pfizer para desarrollar una vacuna. Tras probarla con éxito en ratones, ya han comenzado los ensayos en humanos, con cuatro variantes de un candidato basado en ARN mensajero sintético. Este enfoque múltiple permite realizar una evaluación simultánea para aumentar las posibilidades de identificar al candidato más seguro y eficaz.
- Inovio Pharmaceuticals (Estados Unidos). Fase 1: Este candidato a vacuna, basado en el ARN del virus, comenzó en abril sus primeros ensayos en humanos. Se espera que los primeros datos de la respuesta inmune y posibles efectos secundarios se conozcan a finales de verano. Dependiendo de su éxito, está previsto un ensayo de Fase 2 con una muestra de participantes mucho más amplia.
- Novavax (Estados Unidos). Fase 1/2: La compañía biotecnológica estadounidense acaba de comenzar las pruebas clínicas en humanos con su candidato basado en subunidades proteicas, y espera tener los primeros resultados en julio antes de iniciar la segunda fase. Los investigadores aseguran que los ensayos preclínicos auguran que la vacuna.
- Instituto de Biología Médica (China). Fase 1: El quinto y, de momento, último candidato a vacuna que se está investigando en China abre aún más la puerta a la esperanza, aunque no ha hecho más que comenzar sus ensayos en humanos. Está basado en el virus inactivado.
- Imperial College de Londres (Reino Unido). Fase 1: Científicos de la institución británica acaban de comenzar los primeros ensayos clínicos de una posible vacuna contra la COVID-19. Tal y como han explicado, su proyecto presenta una novedad importante: en lugar de usar una parte del virus, “utiliza hebras sintéticas del material genético del virus, el ARN, empaquetado dentro de pequeñas gotas de grasa”. Alrededor de 300 voluntarios sanos recibirán dos dosis de la vacuna en los ensayos clínicos iniciales, para evaluar si es segura y si produce una respuesta inmune efectiva.
- Gamaleya Research Institute (Rusia). Fase 1: Se trata de una vacuna vectorial combinada contra el coronavirus, y en su desarrollo también participa el Ministerio de Defensa ruso. Las autoridades sanitarias del país ya han comenzado las pruebas clínicas en voluntarios y han anunciado que la producción de la vacuna podría arrancar en otoño.
- Curevac (Alemania). Fase 1: La empresa biofarmacéutica alemana está desarrollando una vacuna ARN que contiene información genética para la construcción de la llamada proteína de espiga del CoV-2 en forma de ácido ribonucleico. La primera fase del estudio clínico ya ha comenzado, en la que participarán 168 voluntarios sanos.
¿Y en España?
A parte de lo que ya se ha señalado al inicio de este post, respecto de los trabajos de investigación en medicamentos terapéuticos, en España hay actualmente reconocidos 10 proyectos de vacuna contra el Covid19, con diferentes aproximaciones conceptuales. Ninguno de ellos ha completado aun la fase PRECLÍNICA.
Son las siguientes:
1. Centro Nacional de Biotecnología (CNB), perteneciente al Consejo Superior de Investigaciones Científicas (CSIC). Ensayos preclínicos con animales de un candidato a vacuna basado en una modificación de la que se usó contra la viruela como vector viral para insertarle genes del nuevo coronavirus que puedan inducir una respuesta inmune adecuada frente al SARS-CoV-2 (Severe Acute Respiratory Syndrome coronavirus 2), que el el tipo de coronavirus causante de la enfermedad comunmente conocida como Covid19. El grupo está liderado por Mariano Esteban y Juan García Arriaza. Utilizando la misma plataforma con la que han trabajado en sistemas inmunizantes para otros proceso víricos (VIH, Chikungunya, Zica) se trata de diseñar una vacuna génica de componentes. Los genes, que el propio organismo traducirá en antígenos, se incorporan en un virus vacuna atenuado, el virus MVA (Ankara modificado) que infecta ingresando en el citoplasma, sin capacidad de reproducirse, actuando como portador de genes ajenos. Este sistema ocasiona simultáneamente dos funciones beneficiosas: por una parte, se comporta como un potente estimulante de la respuesta inmunitaria innata y, por otra, sirve de transporte eficaz de los genes, que se traducen en antígenos específicos, inductores de la inmunidad adaptativa protectora. esta vacuna puede ir rápida en el camino hacia su uso. Será una vacuna complementaria: tras una primo-inoculación con ella, una revacunación con alguno de los otros sistemas asegurará una protección duradera.
2. Centro Nacional de Biotecnología (CNB). En el mismo centro anterior, otro equipo dirigido por Luis Enjuanes e Isabel Sola, trabaja en crear una vacuna a partir de una reconstrucción genética del propio coronavirus vivo, atenuando y eliminando los genes más virulentos mediante ingenería genética. En breve también podrían tener un candidato viable a vacuna. Teóricamente es un inmunógeno ideal. Su camino a través de los ensayos clínicos y aprobación final es, por otra parte, el más dificultoso en razón de la manipulación genética.
3. Centro de Investigaciones Biológicas Margarita Salas, también perteneciente al CSIC. El equipo dirigido por Vicente Larraga está buscando una vacuna que utiliza un antígeno del coronavirus para estimular la inmunidad. El método consiste en colocar el gen del antígeno en un "vehículo" sintético de material genético que pueda ser introducido en el organismo del paciente e inducir la protección frente a la infección. En unas semanas podría empezar a probarse en modelos de ratón. En este caso, la vacuna, también de componentes, está constituida por el ADN de los genes de tres de las partes de las espículas que el virus utiliza para penetrar en las células, insertadas en un plásmido sintético propio del grupo. El plásmido así cargado se incorpora al genoma celular y los RNA mensajeros fabrican los antígenos víricos inductores de la respuesta adaptativa. Ya hay en el mercado una vacuna comercial frente a la Leishmaniosis canina, con esta tecnología, fabricada por una empresa homologada, con lo que el camino habitual hasta su empleo, incluido el último trámite, la fabricación a escala, podría abreviarse.
4. Instituto de Investigaciones Biomédicas August Pi i Sunyer (IDIBAPS) - Hospital Clínico de Barcelona. Proyecto liderado por Felipe García Alcaide, adscrito al Hospital Clínic. En su laboratorio de la Facultad de Farmacia de la Universidad de Santiago de Compostela se va a realizar la fase final: micro-encapsulamiento de la vacuna RNA vírico del SARS-CoV-2. Es este un esfuerzo que aúna fuentes de financiación y centros diversos. Será una vacuna RNA. El diseño computacional se realiza en los centros catalanes citados y departamentos de la Universidad de Barcelona y de la Universidad Pompeu Fabra. Colaborará en la fabricación la Universidad Libre de Bruselas, se transformará en medio aplicable en Santiago de Compostela y se testará en el CNB de Madrid, en animales de experimentación, y en cultivos celulares, en el Clínic.
5. Universidad Ramón Llull. Con el nombre ConiNanoVax, el proyecto busca una vacuna de microARN basada en nanopartículas poliméricas dirigidas a las células dendríticas. Así, estas partículas serían capaces de encapsular material genético y transportar la vacuna hasta las células. El estudio busca desarrollar una respuesta específica para inmunizar a personas sanas pero susceptibles, para protegerlas ante futuras infecciones.
6. Consorcio formado por el Instituto de Investigación del Sida IrsiCaixa, el Barcelona Supercomputing Center y el Centro de Investigación en Sanidad Animal del Instituto de Investigación y Tecnología Agroalimentarias. Está estudiando vacunas mediante VLP (Virus-Like Particles), proteínas virales derivadas de las proteínas estructurales de un virus, que no tienen capacidad infectiva.
7. Universidad de Santiago de Compostela.Coordina el desarrollo de dos proyectos de vacuna, dentro del Centro Singular de Investigación en Química Biolóxica e Materiais Moleculares (CiQUS). El primero de ellos se basa en el ARN mensajero, con la particularidad de que emplea vectores peptídicos para el transporte de material genético. El grupo, liderado por Javier Montenegro, ha desarrollado una alternativa sintética al transporte e incorporación de ácidos nucleicos, en este caso de RNA vírico actuando como mensajero. Desarrollaron una minimolécula proteica híbrida de un lípido y un péptido que actúa como transportador.El trabajo se encuentra aún en fase inicial, pero es bastante original e interesante. El segundo proyecto, lierado por José Martínez Costas, persigue el desarrollo de una vacuna en base a una nueva metodología que induce a que las células fabriquen partículas en las que se pueden introducir los antígenos víricos, que son capaces de estimular al sistema inmune. Es también un proyecto muy original, que cuenta con experiencia práctica ya que, con la misma tecnología desarrollada en el propio centro y patentada por la Universidad de Santiago de Compostela, han conseguido vacunas frente al virus BTV (Ribovirus de la Lengua Azul) y el AHSV (Orbivirus del Peste Equina Africana). A partir de la proteína no estructural muNS, codificada por el gen M3 de un ortoreovirus aviar, identifican y aíslan la porción mínima de esta proteína capaz de expresarse formando inclusiones en ausencia de otros factores víricos, capaces de integrar proteínas diferentes y que se pueden producir en células fúngicas o animales. Las inclusiones así formadas, microesferas de proteína cargadas con los antígenos deseados, se pueden purificar y emplear directamente como antígeno vacunal. Por su constitución física y molecular cuentan con la doble función de estimular el sistema innato e inducir la respuesta humoral y celular adaptativa específica frente al antígeno que transportan (sistema simultáneamente antigénico y adyuvante). El equipo del CiQUS generará la vacuna y los ensayos en animales los llevará a cabo el Centro de Investigación en Sanidad Animal (CISA) de Valdeolmos (INIA, Madrid).
8. Navarrabiomed (Complejo Hospitalario de Navarra) Trabaja en el desarrollo de plataformas de vacunas contra el SARS-CoV-2, un proyecto cuya finalidad es mejorar la ingeniería de posibles vacunas.
9. Instituto Nacional de Investigación y Tecnología Agraria y Alimentaria (INIA) Proyecto basado en un vector a base de plásmidos adaptados e inserciones dobles en el genoma. Su objetivo es utilizar un vector atenuado derivado de la vacuna de la viruela para insertar dos genes del SARS-CoV-2, en una línea similar a la que se está trabajando en el CNB.
10. Universidad de Zaragoza. Trabaja con una posible modificación de una vacuna que ya se está desarrollando contra la tuberculosis, llamada MTBVAC, del grupo de Genética de Micobacterias de la Universidad de Zaragoza, dirigido por Carlos Martín y la empresa Biofabri del grupo ZENDAL. Se encuentra en las fases preclínicas finales, y ahora se está analizando su actividad específica frente al SARS-CoV-2. Se justifica en una de las hipótesis epidemiológicas de la menor incidencia del Covid-19 en las áreas en las que se sigue aplicando como profilaxis de la tuberculosis la vieja BCG (Bacilo Calmette Guérin), dado que la vacuna MTBVAC es una alternativa moderna a la BCG.
- blog de javier.villoslada
- Inicie sesión o regístrese para comentar
